前言:
由十年來的諾貝爾醫學獎得獎紀錄,最近五年得獎的研究領域都集中在『細胞分子學』,生物體的構成基本要素為細胞,而細胞是由分子所組成的,要了解細胞的行為模式就得從分子層面上了解,分子間的交互作用、彼此影響而決定細胞的生長以及分裂,才能更深入的探討生命的運作方法;當然若是調控細胞生長的分子出現了異常,引起不規律的細胞生長及分裂就會引發一些疾病,所以『細胞分子生物學』不僅是探討生命現象,更是將來對抗人類疾病的一個重要利器。
在諾貝爾獎一百週年的日子,2001年的諾貝爾生理醫學獎頒發給三位發現控制細胞複製(cell
cycle)的分子,解開控制細胞分裂機轉,對將來生物醫學有極大幫助的科學家-美國的Leland Hartwell 以及英國的Paul
Nurse和Timothy Hunt。
英美三名科學家因發現細胞分化的重要機轉,為癌症研究開啟關鍵之門,獲得二十一世紀諾貝爾醫學獎第一頂桂冠。無論動物或植物,地球上的所有有機體都是由細胞所組成,因此,揭開細胞演化之謎,是了解生物體何以會成長、病變的起點。
據估計,成年人身上約有一百兆個細胞,奇妙的是,這許多細胞都是從一個受精卵細胞分化而來;而且在人體內,也會不斷有大量新分裂出來的細胞,取代死亡的舊細胞。到底細胞是怎麼分化的?又是那些因素在控制著細胞的分化?
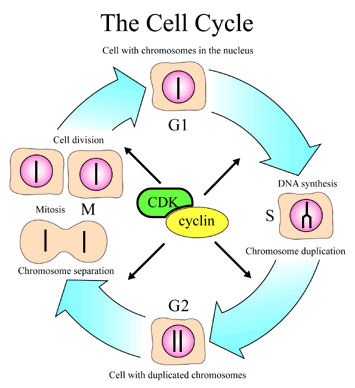
細胞分化周期包含四個階段。第一階段(G1)為複製前期,此時細胞會成長變大,當達到一定尺寸時,細胞就進入分化第二階段(S)複製期,位於細胞核內的去氧核醣核酸(DNA)、染色體會合成複製出一模一樣的一套;到了第三階段(G2)複製後期,細胞會檢查其複製工程是否完備,如果複製完成,就進入第四階段(M)有絲分裂期,染色體會分離開來,原本的細胞也會一分為二,而這兩個細胞便包含完全相同的染色體。
這個細胞分化的過程,在哺乳動物身上,依種類不同,費時約十到三十小時不等。但是,並非所有細胞分化都遵循這種規律,有的細胞在G1期就停滯不前,進入所謂靜止期(G0);有的在不同階段中出了差錯,會造成染色體的變異,可能有某些部分流失、重組、或者在兩個細胞裡不對稱分佈,常見的癌症細胞就是這類不正常分化下的產物。
今年諾貝爾醫學獎得主哈特威爾、韓特、納斯的研究發現,在細胞分化過程中,兩項因素具有關鍵性地位,一是胞轉蛋白(cyclin),一是依賴胞轉蛋白的催化酉每(cyclindependentkinase,簡稱CDK)。
胞轉蛋白是細胞分化過程中必需的蛋白,而其含量會隨分化的循環周期,在不同階段有所不同,並影響CDK的作用。至於CDK則是細胞分化由一個階段轉進到另一階段的關鍵,是由所謂「啟動」的基因所調控。所以,專家形容,CDK就像是汽車引擎,沒有它,細胞分化就不會發生,而胞轉蛋白就像是變速箱,控制著引擎的馬力。
此外,哈威特還提出一個「檢查點(checkpoint)」的觀念,當DNA受損時,細胞會有自然的機制察覺,並停止細胞的分化周期,以便DNA有時間可以修復,再進入下一階段;而這樣的機制,也會確保細胞分化是依照正確的順序在進行。
(1*)
作者介紹:
1、【Leland
Hartwell】
 (4*)
(4*)
利蘭.哈特威爾(Leland Hartwell)現年六十三歲,是美國西雅圖哈金森(Fred
Hutchinson)癌症研究中心的院長,也是西雅圖(Seattle)華盛頓(Washington)大學遺傳學系的教授,1970年代初期開始研究細胞週期的機制,他以酵母菌Saccharymyces
cerevisiae作為研究對象,利用基因突變的技術試圖找出控制細胞週期的關鍵因子,結果篩選出超過一百個調節細胞週期的基因,將它們命名為cdc
(cell division
cycle)基因,其中特別重要的是cdc28基因("start"基因),他發現當此基因突變時細胞週期會停止在G1晚期的"START"關卡,一旦細胞通過"START"關卡便開始進行DNA的複製,因此CDC28蛋白質是一個控制細胞由G1時期進入S時期的重要因子。1980年代,哈特威爾利用高能量輻射線照射酵母菌細胞來研究細胞受到破壞時的反應,因此提出細胞有檢查點(checkpoint)的構想,所謂檢查點是指具有調節功能的蛋白質會在此時期讓細胞週期呈現暫停狀態,讓細胞檢查DNA是否受到破壞或有任何的缺陷,並且在進入下一個時期之前進行修補(repair)的工作,此種構想為目前研究癌細胞分裂增殖為何失去控制提出了一個重要的基本觀念,認為癌症的發生可能與檢查點的調控機制出現問題有關。(2*)
哈特威爾會走入酵母菌遺傳學的研究領域,其實也是一個巧合。在他的求學過程中間並沒有真正的受過任何酵母菌生物學的科學訓練,他在1960年代初從學校畢業後,即跟隨在沙克研究所(Salk Institute)的杜貝克博士(Renato Dulbecco, 1975年諾貝爾生理醫學獎得主)從事有關動物細胞培養及腫瘤病毒複製的博士後研究,因此開始對細胞生長及分裂的調控作用產生興趣。但是苦於動物細胞的複雜度,實驗一直沒有很好的進展。
1965年哈特威爾獲得當時剛成立的加州大學爾灣分校教職聘書,於是離開沙克前往任職。第一年寫了一個研究小計畫,打算繼續利用動物細胞模式來探討細胞分裂調控的問題。可是新學校、新實驗室、加上身為年輕的新老師,哈特威爾的新生涯起步的有點力不從心,光是等待新購的儀器設備抵達就耗掉不少時間。這段時間閒得發慌的哈特威爾只好勤跑圖書館,看看是否能找出更適合的研究題材。當時很多的生物學實驗室已經能夠利用一些黴菌及酵母菌從事各種細胞學及遺傳學上的研究了,發表過的科學報告相當豐富。在一個偶然的機會下哈威爾準備試試酵母菌作為研究材料的可能性。對酵母菌一無所知的他,前往加州大學柏克萊分校及華盛頓大學拜訪了兩位酵母菌學大師—賀松(Donald C. Hawthorne)與羅門(Herschel Roman);向他們討教酵母菌的操作方法,幾天下來彼此交談甚歡,臨走的時候,兩位大師借了他一部顯微鏡及一個酵母菌菌種,哈威爾的酵母菌生涯於焉展開。值得一提的是,當時哈威爾實驗室裡人手奇缺,所有的研究工作都是他帶著幾位大學部學生一點一滴地從收集酵母菌CDC突變種做起;1967年,哈威爾發表了第一篇分析酵母菌細胞分裂突變種的研究報告。(3*)
哈特威爾是開啟酵母菌研究學門宗師,他將研究成果與眾人分享,甚至鼓勵其他科學家慘與,在1970年代,許多科學家都曾收到哈特威爾的信,他在信中原原本本地說明自己酵母菌研究所得的成果,並一一詢問眾人有無興趣投入研究行列,而且只要有人表示興趣,他免費提供研究技術圖片,方便眾人共同研究,大公無私的精神,在競爭激烈的生物醫學界,獨樹一格,也未他贏得『教父』地位。(5*)
2、【Paul Nurse】
 (4*)
(4*)
保羅.納斯(Paul Nurse)現年五十三歲,是英國帝國癌症基金會(Imperial Cancer
Research Fund)的院長,於1975年跟進哈特威爾的研究,以遺傳學與分子方法做細胞週期機制的研究。
納斯所使用的研究工具是另外一種的酵母菌,叫裂殖酵母菌(Schizosaccharomyces
pombe),它和長得卵圓形的出芽酵母菌不一樣的地方是:裂殖酵母菌長成短圓柱狀;而且顧名思義,出芽酵母菌的細胞分裂是以長芽苞的方式,從細胞一旁長出另外一顆細胞來,而裂殖酵母菌的細胞分裂是從長大後的細胞中間裂開形成兩個細胞。(2*)
一般的生物細胞在進行分裂之前一定要經過一段生長的過程,先讓細胞長到足夠的大小才能夠進行分裂,也就是所謂體積管控(size
control)的觀念,這個階段通常發生在細胞分裂的第一個間期(G1),這段時間細胞一方面生長,一方面也同時接受各種生長環境的刺激,諸如生長激素或生長抑制劑的調節作用,決定細胞是否要進行分裂;一旦決定了,細胞接著進入染色體複製期(S
phase),即將所有的遺傳物質複製一份;之後,會有另外一個間期(G2)出現,作為細胞進入有絲分裂的準備期;最後細胞進行有絲分裂(M
phase)產生兩個細胞,各獲得一份完整的染色體。(3*)
於是納斯利用了裂殖酵母菌的特性,不斷地尋找在酵母菌裡決定細胞體積大小的因子,結果找到了一個劃時代的基因—cdc2基因,此基因的功能與cdc28相當,所轉譯的蛋白質不但能控制細胞週期中G2時期進入M時期的檢查點,也能控制G1時期進入S時期的檢查點。進一步對cdc2基因定序之後發現此基因所轉譯的蛋白質是一種蛋白質激脢(protein
kinase),主要是藉由蛋白質的磷酸化來調節細胞週期。1987年,納斯利用具有cdc基因缺陷的酵母菌細胞作為研究細胞週期的工具,藉由送入人類的基因試圖尋找功能與cdc基因相對的人類基因,因此發現了週期素依賴性激脢(cyclin-dependent
kinase 1, cdk1)基因。(2*)
由於此項發現,不單是酵母菌,包含人類在內的各種生物細胞,都依賴著和酵母菌cdc2一樣的基因來決定細胞進行分裂的調節作用。cdc2基因合成的蛋白質是一種叫做蛋白質激脢的酵素,它的作用主要是在當細胞準備進入分裂的時候被活化起來,然後負責磷酸化一些功能性的蛋白質,因而啟動了細胞分裂的機器,一旦細胞完成分裂之後,CDC2的活性馬上受到抑制,必須等到下一次細胞要再分裂的時候,才會再次被活化起來。非常清楚的,納斯的實驗證明了CDC2酵素的活性是決定細胞是否能夠進行細胞分裂的指標。這個突破不僅展現了生物之間存在著生命現象的共通性,更對過去只能在顯微鏡底下觀察的細胞分裂研究工作注入了新的活力;細胞分裂已成為可在試管內藉著酵素活性來分析的實驗了。(3*)
3、【Timothy Hunt】
 (4*)
(4*)
蒂莫‧漢特(Timothy
Hunt)現年五十九歲,是英國帝國癌症基金會(Imperial
Cancer Research Fund)細胞週期研究中心的主任。(2*)他的細胞分裂研究工作主要是利用海膽(sea urchin)的卵做為實驗材料。大量的海膽卵很容易取得,而且就像其它無脊椎和脊椎動物所產生的卵一樣:當卵細胞成熟後,它們都停留在細胞分裂週期的G2時期,一起等待受精作用的發生。一旦接觸到精子的受精作用後,受精卵急速進入下一個有絲分裂期(M phase),並且快速的連續分裂八次,完成初期的胚胎發育工作。因此,動物的卵一直都是研究細胞分裂很好的材料。
韓特在1983年做了一個看似平凡的實驗,他想問一個問題,在這些海膽受精卵分裂的過程中,有沒有任何細胞內的蛋白質會跟隨著細胞分裂的週期性,出現合成或消失的變化?也許這類的蛋白質跟細胞分裂的調控作用就有關聯性。所以他收集了一大批海膽卵,先將它們泡在含放射性胺基酸的溶液中標誌蛋白質,再加入海膽精子給予人工授精,接著隨著細胞分裂的每個時間點收取卵細胞,分析細胞內蛋白質的變化。結果他找到了一種會在細胞進入分裂前大量出現的蛋白質,這個蛋白質緊接著分裂的完成後馬上消失,韓特在當時並不知道這蛋白質的真正功能為何,他將之命名為週期素(cyclin)。
十五年後,CDC2的故事浮現,大家都急著想知道細胞是如何透過CDC2的酵素活性來影響細胞分裂的進行。多方的實驗結果都證明了一件事;單獨存在的CDC2蛋白質其實並沒有酵素活性的存在,它必須要結合另外一個蛋白質以後才有可能被活化。1989年開始的一整個年頭,從酵母菌、果蠅、海膽、青蛙、老鼠、到人類的所有生物模式研究裡共同發現了一個事實,那個需要與CDC2結合,以及會幫助活化CDC2酵素的另外一個蛋白質竟然就是週期素,所以CDC2一下子之間又成了週期素依賴性蛋白質激脢(cyclin-dependent protein
kinase, 簡稱CDK)。因為CDK蛋白質在細胞中是一直都存在的,於是細胞藉著控制週期素的合成及分解,就如同在海膽受精卵中週期素的出現和消失,來控制CDK被活化及抑制的時機而完成細胞分裂的作用
週期素會隨細胞週期而分解,是一個控制細胞週期相當重要的一般性法則(許多蛋白質有其特定時空扮演的角色,當階段性任務完成就遭分解或失去活性。)。漢特之後也在其他動物身上發現週期素,證明該蛋白在生物進化的旅途上相當保守(構造變化不大)與其重要性,至今大約已有10種週期素在人體上發現。在細胞週期各期間,CDK分子的數量是固定的,然而與各式不同的週期素配對結合,便能產生出不同的活性來。如果將cyclin比喻為齒輪組或變速箱,CDK就如同引擎,兩者合力將細胞推過一個又一個的細胞週期,使得生命體得以修復組織或是生生不息的繁衍下去。(5*)
研究成果
利蘭.哈特威爾(Leland Hartwell)、保羅.納斯(Paul Nurse)和蒂莫‧漢特(Timothy
Hunt)的研究發現,在細胞生長分裂的過程中,兩項因素具有關鍵性地位,一是胞轉蛋白(cyclin),一是依賴胞轉蛋白的催化脢(cyclindependentkinase,簡稱CDK)。(5*)
Cyclin是細胞生長分裂過程中必須的蛋白,而其含量會隨生長分裂的循環週期,在不同階段有所不同,並影響CDK的作用至於CDK則是細胞生長分裂由一個階段轉進到另一個階段,是由所謂的『start』的基因所調控,也命名為CDC28,在cell
cycle中,它首先可以控制通過G1 phase過程的基因。所以,專家形容CDK就像是汽車引擎,沒有它,細胞生長分裂就不會發生,而Cyclin就像是變速箱,控制著引擎的馬力。(4*)
此外,利蘭.哈特威爾(Leland Hartwell)還提出一個『check
point』的觀念,的DNA受損時,細胞會有自然的機制察覺,並停止細胞生長分裂週期,以便DNA有時間可以修復,再進入下一階段;這樣的機制,也會確保細胞分化是依照正確的順序進行。
 圖一(4*)
圖一(4*)
如圖一:第一階段(G1)為複製前期,此時細胞會成長變大,當達到一定尺寸時,細胞就進入分化第二階段(S)複製期,位於細胞核內的去氧核醣核酸(DNA)、染色體會合成複製出一模一樣的一套;到了第三階段(G2)複製後期,細胞會檢查其複製工程是否完備,如果複製完成,就進入第四階段(M)有絲分裂期,染色體會分離開來,原本的細胞也會一分為二,而這兩個細胞便包含完全相同的染色體。(1*)

圖二(6*)
如圖二:有許多基因可以調控細胞進入M phase,如suc1以及cdc25,當cdc25基因表現而suc1不表現的時候,cdc2會去磷酸化(dephosphorylation)而與cyclin形成一個複合物,使得促有絲分裂因子(mitosis-promoting factor,MPF)活化,MPF活化而使細胞由G2 phase進入M phase。
進入M phase的cdc2-cyclin複合物會分開,此時只有suc1基因表現的時候,分開的cdc2會磷酸化(phosphorylation)促使分裂完的細胞回覆到G1 phase。
由圖二可知,可調控細胞進入M phase的基因很多,以下介紹調控的基因、其所形成的蛋白質,以及它的功能:(6*)
結語:
今天我們對細胞分裂的瞭解,事實上又往前推展了更大的一步;生物細胞裡頭存在著各種不同類型的CDK及週期素已經陸陸續續地被發掘出來,更重要的,各種實驗顯示,細胞即利用這些不同的CDK及週期素組合,完全掌握了整個細胞分裂週期中每一個步驟的進行;不僅僅是細胞足以進入有絲分裂的管控,甚至細胞在生長中對於外界生長因子的刺激反應,細胞開始複製染色體的時機及過程等等,都取決於細胞內不同的CDK與週期素複合體酵素的活性來管制,因此,從分子生物學的觀點來看,一個生物細胞分裂週期的過程,就相當於是一個CDK與週期素複合體酵素活性的交替循環週期而已。(3*)
因為細胞生長週期的發現,後來其他研究者陸續發現的「腫瘤抑制基因」(可防止細胞失控生長的基因)、「原致癌基因」(原本與細胞正常生長有關,但損壞之後會使細胞失控生長),都可以放在細胞週期的脈絡下思考。最有名的腫瘤抑制蛋白質p53,會在DNA損壞、細胞不正常時大量出現,它會阻擋CDK和週期素複合體的作用,使細胞週期無法進行,壞掉的細胞就不會胡亂生長成癌細胞。
總而言之,現在細胞週期的步驟逐漸解出,等於發現一條新的康莊大道:如果能夠阻止癌細胞無止境地生長,例如阻斷失控的生長步驟,豈不就能殺死癌細胞?除了上述癌症相關明星基因的研究,許多抗癌藥物也針對「CDK抑制劑」方向發展,希望能阻止細胞繼續增生。另外,癌症患者常在療程中接受化學治療,為了殺死癌細胞而施打強力藥劑,連帶使身體上同樣分裂快速的毛囊細胞受傷害,使毛髮快速脫落。研究人員正在發展專一性很高的CDK抑制劑作為新藥,使毛囊細胞降低分裂速度,避免患者嚴重落髮,又不會影響化學藥劑的藥效。(7*)
最後恭喜利蘭.哈特威爾(Leland Hartwell)、保羅.納斯(Paul
Nurse)和蒂莫‧漢特(Timothy Hunt)三位獲得諾貝爾獎,你們的研究成果給予後人極大的收穫,希望你們能再接再厲,恭喜你們。
補充資料:
在這裡補充一些這次諾貝爾獎相關的資料
1、【細胞的有絲分裂】(8*)
有絲分裂是一種細胞分裂的方式,一個母細胞會產生兩個子細胞,擁有與母細胞相同數目和種類的染色體。
有絲分裂的各階段(phases )
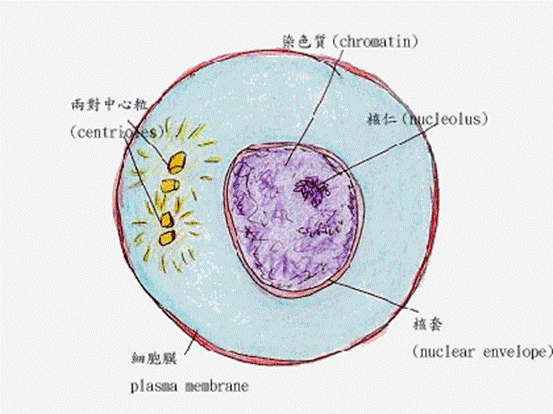
間期 (interphase) : (如圖三)
 圖三
圖三
為有絲分裂中最長的一個階段期,介於連續兩次細胞分裂的中間時期,此時核膜維持完整狀態,而染色體散佈在細胞核;此時細胞除了準備染色體分離外,其他活動皆處於休息狀態。
在間期的G1階段,細胞變大,產生較多的ATP;在細胞具有足夠的ATP,且變的夠大後便會進入S 期;,在S
期細胞會進行DNA的合成;細胞內大部分的物質與能量都在S期中消耗,因此它必須在進入G2時期;。在G2時期細胞再次變大,並產生得到更多的能量,這些能量便被用來進行細胞分裂。在訊號方面,在G1期中,cyclin蛋白質與cdc2蛋白質結合,形成成熟啟動因子(maturation-promoting
factor ,MPF);在S期中cyclin蛋白質被分解,cdc2因此去活化;而後另一個cyclin濃度上升,在
G2期中與cdc2結合形成MPF。
前期 (prophase) :
有絲分裂的第一階段,於此時期分散的染色質(chromatin) 聚集成為染色體
(chromosome)。
其特徵為:1). CyclinB/CDK2蛋白質複合物(為一種kinase),會引發染色質濃縮成染色單體
(chromatid),使其長度變為原來的四分之一。2).細胞核變小且漸漸消失。3).細胞核內的蛋白質合成及液泡運動降到最低。4).
RNA轉錄停止。5).開始組成紡錘絲(mitotic spindle)。有絲分裂的紡錘絲形成其功用有三: 一).
幫助染色體在中期排列成直線;紡錘絲纖維附著在染色體的著絲粒(kinetochore
;著絲粒由蛋白質及RNA所組成的纖維三層構成)上,該紡錘絲纖維稱為著絲粒纖維 (kinetochore fiber)。二).
著絲粒向著細胞兩極,幫助染色體向細胞兩極移動。三). 幫助兩子細胞的細胞核相分離。
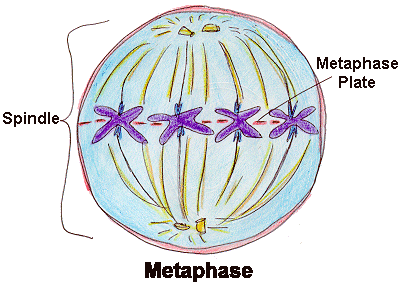
中期 (metaphase) :
有絲分裂的第二階段,於此時期染色體排列於細胞的中央並和兩紡錘極互相垂直。(如圖四)
圖四
其特徵為:1). 細胞膜(nuclear envelope )破裂,形成小囊泡(vesicle)及內質網
(endoplasmic reticulum)。2). 紡錘絲深入細胞核區域及小囊泡盤據於細胞核原區域內。3).
染色體附著到紡錘絲上並向細胞中央移動。4). 染色單體以排成一列的方式向兩極移動。
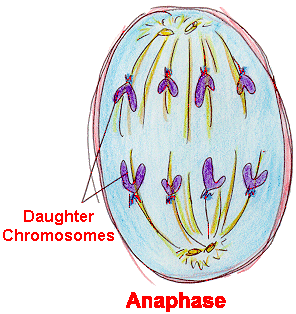
後期 (anaphase) :(如圖五)
圖五
有絲分裂的第三階段,於此時期染色體分開為兩個獨立的姊妹染色單體(sister
chromatids),並各向細胞兩端移動。
其發生之事件為:1).
微管(microtubules)拉曳於染色體之著絲粒上的作用,造成著絲點分離,各染色體的染色單體被拉向它們各自紡錘絲的對應位置。2).
兩極的微管將紡錘絲的兩端拉的更遠。3). 子染色體藉上述二點之作用而分離。4). 微管拉曳作用會持續到所有染色體會合於紡錘絲兩極為止。
末期與質分裂 (telophase and cytokinesis) :
有絲分裂的最後階段,於此時期細胞質分裂為兩部分,核膜再度形成,使得兩個子細胞各自擁有新的細胞核。
在後期中被分成兩群的染色體,在此時會被完全的分開;每一群染色體各自會有新形成的核膜組成之核套圍繞它們,造成兩個新細胞的產生。染色體回復成其絲狀的型態,細胞核分裂的過程至此結束。細胞質分裂(cytokinesis)方面,在動物細胞,細胞於膜處形成凹陷,由actin
與myosin之間相互作用形成。在植物細胞,在兩個分裂中的細胞間會形成細胞板(cell plate),此構造終會變成兩個子細胞的細胞壁。
2、【cyclin和CDK的補充資料】(9*)
圖六
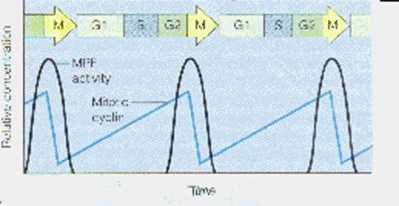
如圖六:在G1、S以及G2 phase時,Mitotic cyclin在細胞內的量是逐漸上升的;進入M
phase後,Mitotic
cyclin的量便逐漸減少,而MPF(促有絲分裂因子)的活性曲線和cyclin的活動是一致的,因為MPF的活性是由於cyclin和CDK結合所造成的,表示說在G2
phase進入M
phase前,cyclin和CDK便已經結合了而造成MPF的活性。「縱軸表示相對濃度、橫軸表示時間、黑線表示MPF的活性、藍線表示Mitosis
cyclin在細胞內的量。」
圖七
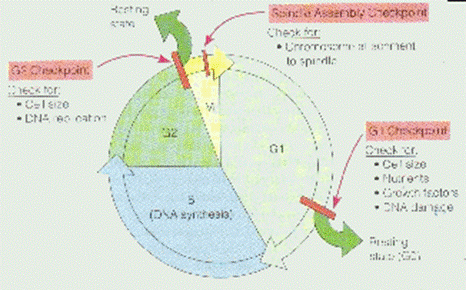
如圖七:Leland
Hartwell提出了『checkpoint,檢查點』,由此圖我們可以知道在真核細胞的細胞週期中,共有三個檢查點,第一個檢查點在G1
phase的晚期,也就是要進入S phase前的檢查點,稱之為G1
Checkpoint,它主要檢查細胞的大小、營養、生長因子,以及DNA是否受損;第二個檢查點在G2 phase的晚期,也就是要進入M
phase前的檢查點,稱之為G2 Checkpoint,它主要檢查細胞的大小和DNA的複製過程是否完全。
在G1 Checkpoint和G2 Checkpoint當中,要是DNA有受損,細胞就會進入Rest
state(G0)(綠色箭頭),待DNA修補完後再進入下一個phase,在M phase的過程中也有一個檢查點,稱之為Spindle Assembly
Checkpoint,它主要檢查然色體是否附著在紡垂體(spindle)上。
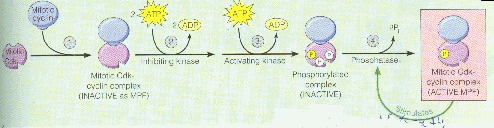
圖八
如圖八:這張圖說明在Cdk-Cyclin複合物的活動→磷酸化(Phosphrylation)、及去磷酸化(dephosphrylation)。
在第一個過程中mitotic
cyclin和Cdk形成一個不具活性的複合物;第二個過程中,兩個抑制的催化脢ATP→ADP產生兩個磷酸群(phosphate
group)(白色的磷酸根)給了複合物,此兩個磷酸群阻礙了複合物的活性位置(active
site);第三個過程中,具有活性的催化脢ATP→ADP給了複合物一個具有活性的磷酸根(黃色的磷酸根),使得複合物形成磷酸化的複合物,此時還不具有活性;第四個過程中,兩個抑制的磷酸群(phosphate
group)(白色的磷酸根)會被移走形成具有活性的磷酸化的複合物繼而活化MPF,此活化的MPF有會刺激被移走的磷酸群(phosphate
group)(白色的磷酸根)去產生另一個有活性的MPF。
(紫色為mitotic Cdk、藍色為mitotic
cyclin、星狀黃色為ATP、橢圓淡黃色為ADP、綠色箭頭為刺激)
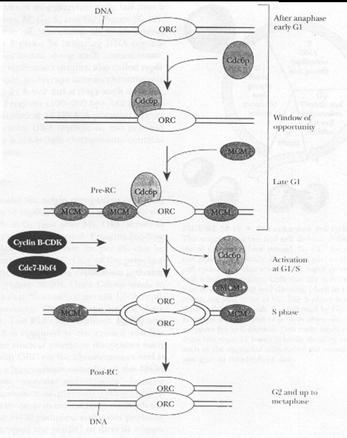
圖九(10*)
如圖九:為在真核細胞中DNA複製週期開始的模式,最初辨識複合物(ORC;origin recognition
complex)在全部的細胞週期複製中都會出現,前複製複合物(pre-RC;pre-replication
complex)為Cdc6p和MCM(複製因子)和ORC結合所形成的複合物,當此複合物受到Cyclin
B-CDK和Cdc-7-Dbf4影響而移除Cdc6p和MCM,此時細胞便由G1 phase進入S
phase,當DNA複製完之後,形成兩個ORC便進入了G2 phase。
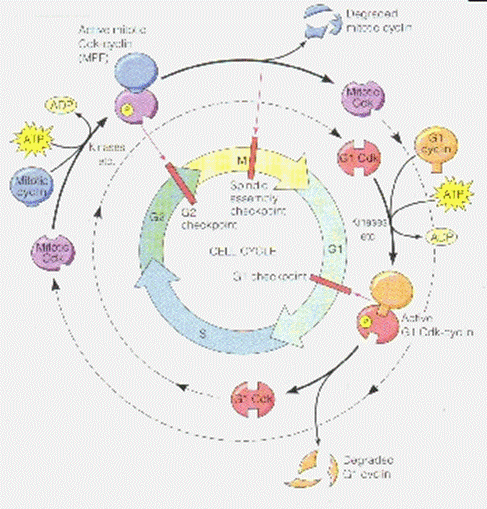
圖十
如圖十:此為細胞週期調控的的模式。根據這個模式,主要的目標蛋白質(triggering proteins)在G1
Checkpoint和G2 Checkpoint中視一個特殊的蛋白質複合物,此複合物是由cyclin和Cdk磷酸化及去磷酸化所形成,磷酸化需要磷酸催化脢;而去磷酸化需要磷酸脢(phosphatase),而且不同的細胞週期時期,有著不同Cdk及其他的基因所調控。
(紅色表示G1 Cdk、橙色表示G1 cyclin、紫色表示mitotic Cdk、藍色表示mitotic
cyclin)
參考資料:
1*http://be1.udnnews.com.tw/2001/10/9/NEWS/MEDICAL/HHLINE/529429.shtm
2*http://www.medlib.ncku.edu.tw/news/2001Nobel.htm
3*http://www.scimonth.com.tw/2001_12/sc_mp_list01.asp
4*http://www.nobel.se/
5*民生報 民國九十年十月九日 星期二 A11版
6*http://www.ndsu.nodak.edu/instruct/mcclean/plsc431/cellcycle/cellcycl1.htm
7*http://www.books.com.tw/onlinepublish/2001100901.htm
8*http://163.14.150.183/old/TOJE/Biology/Contents/Cytology/%E6%9C%89%E7%B5%B2%E5%88%86%E8%A3%82.htm
9* Wayne M.Becker著 “THE WORD OF THE CELL” 2000年第四版
p.566、567、569、572
10*Garrett著 “BIOCHEMISTRY” 1999年第二版 偉華圖書有限公司代理
p.1002、1003