1991年諾貝爾生理醫學獎
得奬者:Erwin Neher and Bert Sakmann
人物簡介:
 內爾(E.Neher) (1944-) 【3】
內爾(E.Neher) (1944-) 【3】
Neher內爾,德國細胞生理學家,與Sakmann薩克曼共同獲得1991年諾貝爾獎。1980年Neher、Sakmann合作發明了patch clamp技術,發現了細胞膜存在離子通道,Neher和Sakmann一起研究基本細胞功能並發揮微區-鉗定技術,這項技術用於檢驗通過細胞膜的極微弱電流的通道。
這一研究成果對於研究細胞功能的調控機制至關重要,可揭示神經系統、肌肉系統、心血管系統及糖尿病等多種疾病的發病機理,並提供治療的新途徑。

薩克曼(B.Sakmann) (1942-) 【3】
Sakmann薩克曼,德國科學家,細胞生理學家,與德國細胞生理學家Neher內爾合作發明了patch clamp技術,發現了細胞膜存在離子通道,而共同獲得1991年諾貝爾獎。該技術是一種廣泛用於細胞生物學及神經科學研究的方法,可藉以檢驗小至一萬億分之一安培的通過細胞膜的電流。
他與Neher同在一個實驗室,他們一道最終確認了細胞膜上離子通道的存在,離子通道是一些具特徵性的機制,有的僅允許陽離子通過,有的僅允許陰離子通過,接著他們研究了多種細胞功能,終於發現離子通道在糖尿病、癲癇、某些心血管病.某些神經肌肉疾病中所引起的作用,這些發現使研究新的更爲特異性的藥物療法成爲可能。
得獎內容:發現細胞的單一離子通道之功能
for their
discoveries concerning "the function of single ion channels in
cells".
1991年諾貝爾醫學獎頒給了德國的兩位生理學家Erwin Neher和Bert Sakmann。其實這對生物物理學界而言並不覺得訝異。因爲自1976年他們發明了「單一離子通道記錄法」(single
channel recording or patch clamp recording),即對神經科學及細胞生物學界産生了革命性的影響。
生物體內的各種細胞由於周遭離子分佈的不均勻,因此在平常靜止狀態時,細胞內所帶的電荷是“-"的,而細胞外通常是比較“+"的,這就是所謂的靜止膜電位(resting membrane potential)。當細胞興奮時如神經的傳導,肌肉的收縮或腺細胞的分泌,細胞膜上的離子通道(如Na+
channel)就會打開,讓Na+離子由細胞外進入細胞內産生去極化現象(Depolarization)。
因此要瞭解神經細胞間訊息的傳遞及肌肉細胞收縮的原理,首先就是要探討細胞膜上各種離子通道如何選擇性的運送離子。Neher和Sakmann使用微細之玻璃電極緊密地吸附著肌細胞膜而精確測量到單一離子通道的電流變化,使我們更清礎離子通道本身開關之機轉及調控困素。由於patch
clamp技術之發明,使我們對一些疾病之病因有深層的認識。例如cystic fibrosis是由於氯離子通道(chloride channels)産生病變而造成。
同時利用patch clamp之方法,可更精確測量到中樞神經細胞所産生之微小興奮性神經突電位(miniature excitatory
postsynapticpotential(mEPSP))。使我們對腦中記憶和學習形成過程有更進一步的瞭解。
總之,由於patch clamp方法之發明,使我們更清楚知道細胞膜離子流動及細胞功能之關聯。對於生命之奧妙及疾病病因之探討,有了劃時代的進展。 【5】
離子通道
1991年10月7日年諾貝爾獎金頒獎大會上,諾貝爾生理學獎授予給了Erwin Neher and Bert Sakman因爲他們的重大成就-----細胞膜上單一離子通道的的發現。
細胞是通過細胞膜與外界隔離的,在細胞膜上有很多通道,細胞就是通過這些通道與外界進行物質交換的。這些通道由單個分子或多個分子組成,允許一些離子通過。通道的調節影響到細胞的生命和功能。Erwin Neher 和Bert Sakmann合作,結果發現當離子通過細胞膜上的離子通道的時候,産生十分微弱的電流。Neher
and Sakmann在實驗中,利用與離子通道直徑近似的鈉離子或氯離子,最後達到共識:離子通道是存在的,以及它們如何發揮功能的。有一些離子通道上有接受體,他們甚至發現了這些接受體在通道分子中的定位。【1】
Summary 摘要
所有的活細胞都有一層膜所包圍著,以隔絕細胞的內外界。在這層膜上,有通道蛋白(channels)作為細胞與周圍環境的連通管道。這種channels由單一的分子或分子複合物所組成,有允許帶電原子-離子(ions)通過的能力。離子通道(ion channels)的調節會影響細胞的生存,也會影響其在正常情況或受病原感染的情況下應有的功能。1991年的諾貝爾生理醫學獎授予了ion channels功能的發現。兩位德國細胞生理學家Erwin Neher和Bert Sakmann一起找出了以極微小電流(總計一個picoampere - 10-12A)通過單一ion channel之技術。這個技術是獨一無二的,因為它表示了單一通道分子需如何改變構形,以及在以百萬分之一秒計數的時間單位內,是如何控制內部的電流活動。
Neher和Sakmann決定性地建構了這個技術 - ion channels的存在以及其作用方式。他們證實了與單一鈉離子或是氯離子有關的情況下,對ion channel開啟或關閉有何影響。有些ion
channels是由位於通道分子一邊的接受體(receptor)所調節的,端賴其形狀活化與否。Neher和Sakmann證明了部分分子可作為感知器(sensor),以及作為channel的內壁。他們也證明出通道蛋白是如何調節正、負荷電荷離子的通行。這項新知及其分析方法是過去十年來現代生物學的重大變革,可促進學術研究,並且有助於對一些疾病其胞內機制的了解,例如糖尿病(diabetes)和囊胞性纖維症(cystic fibrosis)。
What Happens Inside the Cell?
細胞內到底發生了何事?
細胞膜內是一個被限定良好的環境,有許多複雜的生化反應在此發生。細胞內部與外界有極大的不同。例如其所含有的帶正電之鈉離子和鉀離子,以及帶負電的氯離子都相當的不同。由於電荷離子的不同,會導致細胞膜上的電壓強度有0.03到0.1伏特的不同。這通常稱為膜電位(membrane potential)。細胞改變膜電位的方式有數種。其可藉著快速地開啟鈉離子通道,膜電位可在千一分一秒內完全改變。細胞在神經系統中用電訊號的方式快速地延著神經突起傳遞以互相連繫。當電流到達兩細胞的交會點 – 突觸(synapse) – 會誘導神經傳遞物質的釋出。這種物質會影響標的細胞(target cell)上的接受體,通常藉著開啟的離子通道來影響。膜電位藉此改變,表示細胞被刺激或是抑制了。神經系統包含了一連串神經細胞所組成的神經網路,而神經細胞中的不同功能是由突觸所連結的。大腦中新的記憶軌跡就是由改變位在神經網路突觸上的離子通道數目所決定的。所有的細胞功能都是以相同方式來產生的。事實上,生命就是由改變膜電位而開始的。當受精時精子與卵子融子融合在一起,離子通道便立即被活化了。這種結果會改變膜電位,以防止其他精子細胞接近、進入。所有的細胞 – 例如神經細胞、腺細胞、以及血液細胞 – 皆有獨特的一套離子通道,使其有能力執行特定功能。離子通道是由單一分子或是分子複合物所構成,形成了通道壁或通道孔 – 以穿透過細胞膜並連接細胞的內外環境。(Figure 1B and 1D)。通道孔的直徑非常小,但可讓單一的離子通過(0.5-0.6 millionths of a millimetre)。分子形狀若立即改變,即代表離子通道開啟或關閉。這只有藉著特定的訊號分子活化分子某部位上的接受體(Figure 1D)才會發生。交替地改變分子特殊部位的膜電位,可以開啟或關閉離子通道。
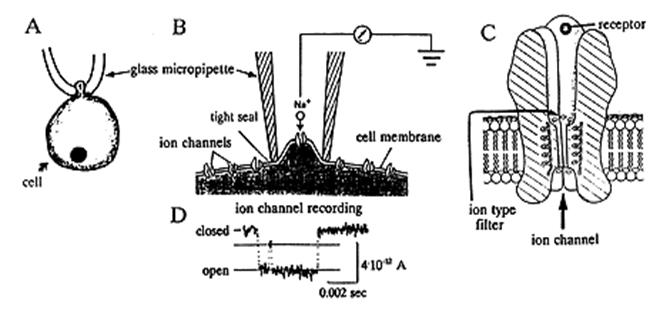
Figure 1. Neher和Sakmann使用記錄電儀來記錄單一離子通道的電流。A 圖中顯示出玻璃微量吸管(glass micropipette)接觸進入至細胞中,圖B,則是使用高級放大儀,將膜上的離子通道與微量吸管的尖端相觸,以放大一部分的細胞膜。其中,微量吸管內連接了電流放大器。D,表示電流通過離子通道,離子通道開啟。C為通道的高度放大:細胞外覆著接受體以及離子瀘器(ion filter)。
Neher and Sakmann Record the Electric Current Flowing Through a
Single Ion Channel
Neher和Sakmann記錄了流經單一離子通道的電流
已知細胞膜上的離子改變是快速的,但Neher和Sakmann是第一發現有特殊的離子通道實際存在。為了說明離子通道的作用方式,所以必須記錄通道是如何開啟和閉合的。流經單一離子通道的離子性電流十分微小,這似乎難以證明前述情況。此外,有小的離子通道分子嵌在細胞膜上。Neher和Sakmann成功地解決了這些困難點。他們發明了細小的玻璃微量吸管(直徑為a thousandths of a millimeter)作為記錄電極。當微量吸管接觸進入細胞膜,微量吸管的孔洞周圍會形成緊實的密封狀(Figure 1A, B)。微量吸管內外部的離子改變,僅發生在膜上的離子通道。當單一的離子通道開啟,帶電的離子將會移動通過離子通道,形成電流。經過精密的電子設備,他們成功地估量出實驗中的精微電流(”microscopical” current)。
How Does an Ion Channel Operate?
離子通道是如何運作的?
離子通道有數種不同的型態。有些只充許帶正電的離子通過,例如鈉離子、鉀離子、或鈣離子等,有的只充許陰離子通過,如氯離子。Neher和Sakmann發現了這種特異性是很完備的。其中一個原因是由於離子通道的直徑大小,僅適於一特定離子的直徑。其中一型的離子通道,具有兩個帶有正荷或是兩個負荷胺基酸的環。這種環形成了離子濾器(see
Figure 1C),只充許一個相反電荷的離子通過這個濾器。特別的是,Sakmann和其他不同的分子生物學一樣,完成了一個具創造性的反應,這個反應解釋了離子通道分子的不同部分是如何運作的。Neher和Sakmann的科學成就徹底地改變了我們在細胞功能上的觀點,以及細胞生物學教科書上的內容。如今,他們的方法被世界上數以千計的科學家廣泛使用。
The Study of Secretory Processes
分泌過程進行之研究
神經細胞和產生荷爾蒙的細胞一樣,會在host defence(例如mast cells)分泌出不同的作用物質。這些物質是儲藏在膜包圍的囊泡中。當細胞受刺激,囊泡便會向細胞表面移動。細胞膜與囊泡的膜融合,游離出作用物質。Mast cell會分泌組織胺(histamine)和其他作用物質,以提高局部性的發炎反應。腎上腺髓質細胞則會游離出壓力作用荷爾蒙 – adrenaline,胰臟的beta cells則分泌胰島素(insulin)。Neher說明了這些細胞種類的分泌過程,暨而發明出一種新的技術,以記錄囊泡與細胞膜之融合。Neher了解若是細胞表面狀況改變了,將會影響細胞的電性質,如此就有可能記錄到實際的分泌過程。他們進一步設計了複雜的設備,最後,如何記錄與細胞膜融合的小囊泡之方法已被解答。
Regulation on Channel Function
離子通道的調節功能
Neher和Sakmann也使用微量吸管電極將不同的作用物質注射到細胞內,因此研究出細胞分泌不同的階段。在這個方法中,說明了細胞分泌的機制為cyclic AMP或是鈣離子所擔任的。例如,現在我們已較了解荷爾蒙在血液中的量是有某種程度的維持度。胰島素分泌的基礎機制也已被證實。血液葡萄糖的濃度控制了insulin-forming cell的細胞內葡萄糖濃度,然後依次再去調節ATP這個能量物質。ATP會直接作用在特定種類的離子通道,以控制細胞的膜電位。然後,膜電位的改變會直接影響其他的離子通道,以充許鈣離子通過細胞。鈣離子隨後會引發胰島素的分泌。糖尿病患的胰鳥素分泌則是發生紊亂的。某些藥物可直接作用在被ATP所控制的離子通道(ATP-controlled ion
channels)上,用以刺激糖尿病患的胰島素分泌,許多疾病是完全、或部分地由於離子通道的調節有缺陷所致,而有些藥物則可直接作用在離子通道上。許多病理機制經過這些離子通道的研究顯得更清楚,例如囊胞性纖維症(氯離子通道)、癲癇症(鈉離子和鉀離子通道)、一些心血管疾病(鈣離子通道)、以及像是Lambert-Eatons疾病類的神經肌肉失序(鈣離子通道)等。在Neher和Sakmann發明這種技術的幫助下,現在可以專門設計一些藥物,以最有效的方式作用在影響某疾病的特定離子通道上。例如抗焦慮的藥物會作用在大腦的抑制性離子通道。酒精、尼古丁、以及其他毒物也會作用在一些離子通道上。總結而言,Neher和Sakmann的研究貢獻是對細胞生物上的一種革命性改變,並用以了解不同疾病的作用機制,開啟了一個發展新藥物的方式。【2】
一把研究利刃【6】
從前在研究細胞離子通道時,多仰賴一些電生理的技術,像插入一根電極到細胞內,然後連通另外一個在細胞外的電極,記錄不同生理情況的細胞膜電位差變化。但是這種傳統電生理的技術解析度不夠,而且沒有辦法任意改變細胞內的各種成分,再觀察這些改變對細胞膜上離子通道的影響。然而,這些難題在Neher和Sakmann發展出“patch clamp”技術後,便都迎刃而解。
他們利用一個毛細玻璃管,管口的直徑比一個細胞還小,大約只有二到三微米(10-6米)。如果這個毛細管口非常乾淨,在顯微鏡底下將它輕輕壓位細胞的表面,再加點吸力,細胞膜就會緊緊黏在管口上。如果細胞膜上有一個離子通道的分子,經過電流的記錄儀器,就可以記錄在這個離子通道進出的離子流。
這方法說來容易,做起來卻需要很大的耐性與細心。但是Neher和Sakmann在1976年終於應用這套技術,順利地記錄出青蛙肌肉細胞上單一離子通道流過電流的大小。在此之前,大家很難了解細胞膜內外離子的變化,究竟是透過少數幾個能通過大量離子的通道,還是經由許多只會通過少量離子的通道。Neher和Sakmann的結果顯示,肌肉細胞的細胞膜上一個離子通道可通過的電流約為二十微微安培(10-12安培),換成離子數目大約是每秒通過一億個離子。
Figure
2用一個真實例子說明,利用patch clamp測定單一乙醯膽鹼後,可看到管道立刻打開引入離子流(鈉離子鉀離子,見Figure 2A),而且離子管道有一定開放的大小(見Figure 2B),隨後離子管道很快關閉(見Figure 2C),而在開放期間會不定期地關閉。這個結果顯示:離子通道的蛋白可能存在「開」和「閉」二種不同的狀,而乙醯膽鹼與receptor結合後,可在千分之一秒內讓通道從一個狀態跳到另一個狀態。從橫坐標可以看出離子通道開閉的過程,緃坐標則表示離子通道流的大小。
Patch
clamp技術除了告訴我們,細胞膜上有各式各樣的離子通道(大約二十到四十種)外,它還能告訴我們,這些離子通道如何因應不同的環境而改變其特性。換句話說,離子通道並非一成不變。組成通道的蛋白質在不同環境下,會改變形態,造成離子流量的變化,譬如 說胰臟分泌胰島素,就是受到胰島細胞膜離子通道的影響;利用patch clamp技術,科學家發現,這些離子通道和胰島細胞內能量的供應有關。能量供應愈充分,表示血液中糖分濃度愈高,透過離子通道的調節,可以促成胰島細胞釋放胰島素來降低血中的糖分。
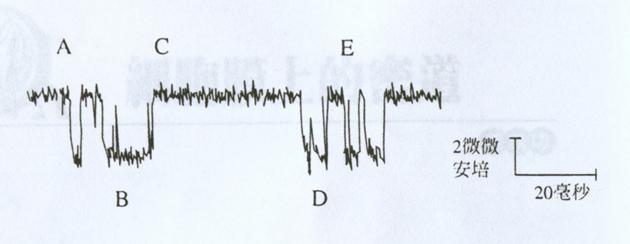
Figure 2. 利用patch clamp技術,測定單一乙醯膽鹼receptor通道表現的記錄。
單離子通道記錄法之發明
1991年諾貝爾醫學獎頒給了德國的兩位生理學家Erwin Neher和Bert Sakmann。其實這對生物物理學界而言並不覺得訝異。因為自1976年他們發明了「單離子通道記錄法」(single
channel recording or patch clamp recording),即對神經科學及細胞生物學界產生了革命性的影響。
生物體內的各種細胞由於周遭離子分佈的不均勻,因此在平常靜止狀態時,細胞內所帶的電荷是“-”的,而細胞外通常是比較“+”的,這就是所謂的靜止膜電位(resting membrane potential)。當細胞興奮時如神經的傳導,肌肉的收縮或腺細胞的分泌,細胞膜上的離子通道(如Na+
channel)就會打開,讓Na+離子由細胞外進入細胞內產生去極化現象(Depolarization)。
因此要瞭解神經細胞間訊息的傳遞及肌肉細胞收縮的原理,首先就是要探討細胞膜上各種離子通道如何選擇性的運送離子。Neher和Sakmann使用微細之玻璃電極緊密地吸附著肌細胞膜而精確測量到單一離子通道的電流變化,使我們更清礎離子通道本身開關之機轉及調控困素。由於patch
clamp技術之發明,使我們對一些疾病之病因有深層的認識。例如cystic fibrosis是由於氯離子通道(chloride channels)產生病變而造成。
同時利用patch clamp之方法,可更精確測量到中樞神經細胞所產生之微小興奮性神經突電位(miniature
excitatory postsynaptic potential(mEPSP))。使我們對腦中記憶和學習形成過程有更進一步的瞭解。
總之,由於patch clamp方法之發明,使我們更清楚知道細胞膜離子流動及細胞功能之關聯。對於生命之奧妙及疾病病因之探討,有了劃時代的進展。
Patch clamp
recording之重要性
1.可精確量到單一離子通道之電流變化。對於single channel開關之動力學可作更深入之探討。
2.可適用於各種細胞如肝腎、心、淋巴球及腦神經細胞,對於細胞膜上離子通道之性質和疾病病因產生之關聯性,開啟了劃時代的進展。
3.使用cell attached patch clamp之方法可研究receptorsecondary
messengers對ion channel之調控作用。
4.使用whole cell recording及Inside-out
patch方法可直接看藥物或secondary messengers在細胞內之作用。
5.對於較小之細胞如腦神經細胞,比傳統之細胞內記錄法(intracellular
recording)容易學,而且設備並不昂貴。
6.可同時作patch clamp量電流,並用Fluorescence
microscope及current之變化,細胞內〔Ca++〕濃度之改變與細胞功能之關聯性。
追踪疾病成因【6】
Patch
clamp能幫我們了解一些疾病的成因。譬如說遺傳疾病cystic fibrosis,在白種人中的罹患率非常高,而患者很少能活到成年。這種病人的汗水中有高濃度的鈉和氯離子,且肺中常分泌大量黏液而引起呼吸道感染。此外,病人的小腸等器官也會出現黏液分泌異常。這種病的成因一直到patch
clamp技術出現後,才鑑定出是由於病人細胞膜上氯離子通道完全不見,或是功能異常所致。進入1990年代後,科學家更是利用基因工程方法,鑑定出病人損壞的基因,的確就是細胞膜上的氯離子通道。
了解了細胞離子通道的特性後,就可設計一些特殊的藥物來控制這些通道的開關,進而調整細胞整體的功能。另一方面我們也可以透過離子通道,來認識細胞在不同環境中應對的機制。所以patch
clamp技術對現代生物學的衝擊是很大的,這也是另一個因技術突破而引發重大科學進展的例子。
生物物理學家Neher和生理學家Sakmann,在細胞研究方面開啟了新紀元。他們慷慨地將patch
clamp技術公開,敞開實驗室的大門,歡迎世人來分享。
Reference出處
【1】 醫學八號樓/ 諾貝爾生理或醫學獎/ http://www.med8th.com/nobel/winners/1991/about-ionchannels.htm
【2】 Nobel
e-Museum/ http://www.nobel.se/medicine/laureates/1991/press.html
【3】 中國科普/ 科學人物/ Sakmann/ http://www.cpus.gov.cn/kxrw/index.asp?rw=377&jiang=69
Naher/ http://www.cpus.gov.cn/kxrw/index.asp?rw=376&jiang=69
【4】 成大醫學院圖書館/ 1991諾貝爾醫學獎得主/ http://www.medlib.ncku.edu.tw/people/1991.html
【5】 哈爾濱工業大學/ 歷屆諾貝爾生理醫學獎/ http://www.hit.edu.cn/gongdaxw/kejiyuan/NOBEL/medicine/medicine.htm
【6】 諾貝爾的榮耀-生理醫學桂冠/ 科學月刊 著/ 天下文化書坊/ P70~74